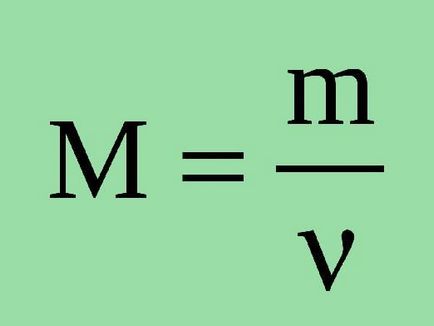
În chimie nu se poate face fără o mulțime de substanțe. La urma urmei, acesta este unul dintre cei mai importanți parametri ai unui element chimic. Vă vom spune cum să găsiți masa materiei în diferite moduri în acest articol.
În primul rând, trebuie să găsiți elementul potrivit utilizând tabelul Mendeleyev, pe care îl puteți descărca pe Internet sau cumpăra. Numerele fracționare sub semnul elementului sunt masa atomică. Aceasta trebuie să fie înmulțită cu indicele. Indicele arată câte molecule ale elementului sunt conținute într-o anumită substanță.
- Când aveți o substanță complexă, trebuie să multiplicați masa atomică a fiecărui element al materiei prin indicele său. Acum este necesar să adăugați masele atomice primite de dvs. O astfel de masă este măsurată în unități de gram / mol (g / mol). Cum găsim masa molară a unei substanțe, arătăm pe exemplul de calcul al greutății moleculare a acidului sulfuric și a apei:
H2S04 = (H) * 2 + (S) + (O) * 4 = 1 * 2 + 32 + 16 * 4 = 98 g / mol;
H2O = (H) * 2 + (O) = 1 * 2 + 16 = 18 g / mol.
Masa molară a substanțelor simple, care constă dintr-un singur element, se calculează în același mod.
Atunci când, de exemplu, cunoașteți volumul, presiunea, masa și temperatura în grade Kelvin (dacă este C apoi tradus), învață cum să găsească substanțele cu greutate moleculară pot, folosind ecuația lui Mendeleev-Clapeyron:
unde R este constanta de gaz universal - M este masa moleculara (molara), amu.
unde n este cantitatea de substanță-m este masa substanței. Aici este necesar să se exprime cantitatea de materie în volum (n = V / VM) sau numărul lui Avogadro (n = N / NA).
M = P1 * Ek * (1000 / P2 * tk),
unde P1 - este greutatea solut, r P2 - este greutatea solventului, r Ek - această constantă cryoscopic a solventului, care poate fi găsit în tabelul corespunzător. Această constantă este diferită pentru diferite lichide - tk este diferența de temperatură, care este măsurată cu un termometru.
Acum știi cum să găsești o masă de materie, simplă sau complexă, în orice stare agregată.